吴云东课题组在蛋白质力场发展上取得突破性进展
北京大学深圳研究生院吴云东院士课题组近日在《The Journal of Physical Chemistry Letters》(物理化学快报,Nature Index期刊,IF=9.35)上发表文章 “Significantly Improved Protein Folding Thermodynamics Using a Dispersion-Corrected Water Model and a New Residue-Specific Force Field”。
文章链接:http://pubs.acs.org/doi/abs/10.1021/acs.jpclett.7b01213
分子动力学(MD)模拟已经成为研究生物分子结构和功能的重要手段,其物理模型是基于描述原子间相互作用的势能函数(分子力场)。近年来,随着计算机性能以及研究体系复杂程度的不断提高,对分子力场的精度要求也在逐渐提高。然而,近年来的研究发现,目前常用的分子力场并不能很好地描述蛋白质折叠-去折叠平衡的温度依赖性,而且模拟中的非折叠态的构象具有明显的塌缩倾向,通常会得到与实验结果相比更小的回转半径。这些问题都表明当前的分子力场在准确性上仍然存在着一定的缺陷,阻碍了MD模拟在蛋白质结构和功能研究中的进一步应用,尤其是对天然无序蛋白质和蛋白质折叠过程的模拟。因此,发展能够同时准确地描述蛋白质不同状态的蛋白质分子力场和水分子模型仍是该领域的重要问题之一。
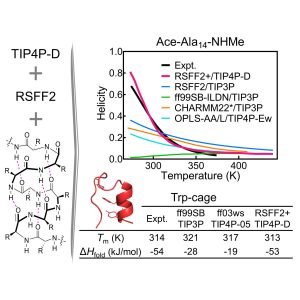
该工作在本课题组自主发展的残基特异性蛋白力场RSFF2的基础上,通过对α-螺旋氢键的进行能量修正,引入部分多体效应的影响,得到新的RSFF2+力场。该力场与新的TIP4P-D水模型搭配使用,能够显著改善蛋白质在不同温度下折叠态和非折叠态的热力学平衡问题,很好地重现实验测量的蛋白质折叠热力学数据。除此之外,这一方法还能够在不影响蛋白质天然态结构的情况下得到更加合理的非折叠态构象分布,同时实现了对具有特定三维结构的蛋白质和天然无序蛋白质的准确模拟。这一成果在一定程度上解决了以往的分子力场在描述蛋白质不同状态时存在的普遍问题,为蛋白质力场和水模型的发展提供了理论基础和新的思路。
本研究由吴云东和蒋帆共同指导博士研究生吴昊南完成。该工作得到了国家自然科学基金,广东省领军人才专项基金和深圳市科技创新委员会的支持。